Sodium bisulfite là gì ? Có phải đây là hóa chất chuyên tẩy trắng không ? Đây luôn là những câu hỏi người dùng cần được tư vấn tước khi mua sản phẩm hóa chất này. Vậy rốt cuộc đây là hóa chất gì ? Chúng có công dụng ra sao ? Hãy tìm hiểu bài viết dưới đây để rõ hơn nhé.
1. Sodium Bisulfite Là Gì ? Cấu Tạo Phân Tử Của Sodium Bisulfite
1.1. Sodium Bisulfite là gì ?
Sodium bisulfite là một muối của axit sulfuric, hay còn được gọi với các tên gọi khác như Natri Bisulfite, Sodium Hydrogen Sulfite… Đây là hóa chất có công thức hóa học tổng quát là NaHSO3. Chúng tồn tại dưới dạng hợp chất có dạng tinh thể rắn, màu trắng, ngoại quan khá giống đường cát trắng. Nó tan trong nước và không cháy được.
Về điều chế, nó được tạo thành khi một phân tử axit sulfuric (H₂SO₄) phản ứng với một phân tử natri hydroxit (NaOH). Sodium Bisulfite rất đa năng, thường được sử dụng trong các ngành công nghiệp và hóa chất với nhiều mục đích khác nhau. Các bạn lưu ý Sodium Bisulfite là một chất có tính axit nhẹ và có thể gây kích ứng da và mắt nếu tiếp xúc trực tiếp.

1.2. Cấu tạo phân tử của NaHSO3
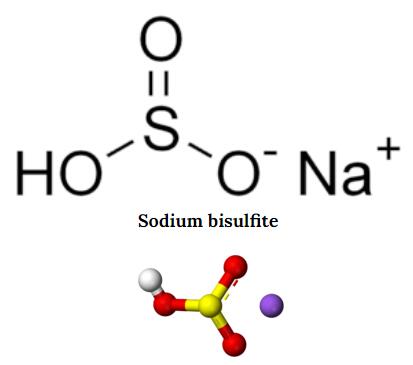
2. Tính Chất Vật Lý và Hóa Học Của Sodium Bisulfite
2.1. Tính chất vật lý
- Natri Bisulfite tồn tại dưới dạng là một chất rắn màu trắng
- Khối lượng riêng của Natri Bisulfite là 1.48 g/cm3
- Khối lượng mol là 104.061 g/mol
- Natri Bisulfite không cháy, vị khó chịu và tan trong nước
- Độ nóng chảy của Sodium Bisulfite ở 150 ° C (302 ° F, 423 K)
- Điểm sôi tầm 15 ° C (599 ° F, 588 K)
2.2. Tính chất hóa học
- Natri Bisulfite có thể tác dụng với kim loại theo phương trình minh họa sau:
Zn + 2NaHSO3 ⟶ Zn(OH)2 + Na2S2O4 - Còn khi cho Natri Bisulfite tác dụng với axit Sunfuric kết quả sẽ sinh ra khí mùi hắc chính là Lưu huỳnh đioxit (SO2) làm sủi bọt khí
H2SO4 + NaHSO3 ⟶ H2O + SO2 + NaHSO4 - Bên cạnh đó nó cũng có thể tác dụng với một bazơ
Ba(OH)2 + 2NaHSO3 ⟶ 2H2O + Na2SO3 + BaSO3 - Ngoài ra khi cho Natri Bisulfite tác dụng với Phenol phương trình sẽ là
C6H5OH + NaHSO3 ⟶ C6H5ONa + H2O + SO2 - Khi cho Sodium bisulfite kết hợp với thuốc tẩy clo (NaClO loãng) sẽ giảm thiểu được hơi độc.
NaClO + NaHSO3 ⟶ NaCl + NaHSO4 - Sodium bisulfite khi bị phân hủy sẽ tạo thành nước, khí lưu huỳnh đioxit và muối của natri như sau:
2NaHSO3 ⟶ H2O + Na2SO3 + SO2
3. Cách Điều Chế Sodium Bisulfite
Thực tế, có nhiều cách để điều chế Sodium bisulfite nhưng 2 phương pháp dưới đây là được áp dụng phổ biến nhất…
- Điều Chế Natri bisulfite bằng phương pháp sục khí lưu huỳnh đioxit dư vào dung dịch natri hydroxit
SO2 + NaOH → NaHSO3 - Ngoài ra cũng có thể sục lưu huỳnh đioxit vào dung dịch natri cacbonat để điều chế NaHSO3
2 SO2 + Na2CO3 + H2O → 2 NaHSO3 + CO2

4. Ứng Dụng Của Sodium Bisulfite
Hóa chất Natri bisulfite NaHSO3 nổi tiếng với khả năng khử và tẩy. Nó đóng vai trò như một chất khử, chất tẩy trắng được ứng dụng đa dạng trong nhiều ngành công nghiệp khác nhau. Điển hình như:
- Là chất khử trong các ngành sản xuất thuốc nhuộm, giấy, dệt may, thuộc da, công nghiệp tổng hợp hóa học
- Trong ngành công nghiệp dược phẩm: NaHSO3 dùng để sản xuất dipyrone và trung gian aminopyrine.
- Natri bisulfite được dùng để xử lý nước thải có chứa các thành phần như crom, clo… Và khử trùng nước trong một số ứng dụng công nghiệp.
- Là một phụ gia đặc trưng riêng biệt trong ngành công nghiệp xi mạ
- Bảo quản thực phẩm: giúp ngăn ngừa sự phát triển của vi khuẩn và nấm mốc.
- Đây là một tác nhân khử mạnh mẽ, thường được sử dụng trong các phản ứng hóa học để giảm các hợp chất oxy hóa. Vì nó phản ứng dễ dàng với oxi: 2NaHSO3+O2 --> 2Na+ + 2H+ + SO4 -2 . Nó thường được thêm vào các hệ thống ống dẫn lớn để ngăn ngừa sự ăn mòn oxi hoá. Trong công trình hoá sinh, nó giúp duy trì điều kiện thiếu không khí trong lò phản ứng.
5. Những Lưu Ý Khi Sử Dụng Natri Bisulfite
- Natri bisulfite- NaHSO3 có tính axit nhẹ, có thể gây kích ứng da và mắt. Từ đó, làm tổn thương cho giác mạc, dẫn đến mù lòa. Hãy mang dụng cụ bảo hộ như đeo găng tay, kính bảo vệ và các trang thiết bị bảo hộ khác nếu cần thiết.
- Natri Bisulfite là một chất khử mạnh và có thể tham gia vào các phản ứng hóa học với các chất oxy hóa mạnh, gây ra phản ứng mạnh hoặc tạo ra nhiệt. Không nên kết hợp nó với các hóa chất như axit mạnh, clo hoặc các chất có tính oxy hóa khác
- Không nuốt phải hay hít phải hóa chất. Khi hít phải Natri bisulfite có thể gây hại cho hệ hô hấp với các triệu chứng điển hình như ho, thở khò khè, thở ngắn.
- Nếu vô tình nuốt phải NaHSO3 sẽ xảy ra các triệu chứng như buồn nôn, tiêu chảy, đau bụng, xuất huyết dạ dày. Nếu vô tình nuốt phải hoặc hít phải, cần phải tìm kiếm sự trợ giúp y tế ngay lập tức.
- NaHSO3 khi tiếp xúc với thời gian dài có thể gây nên hen suyễn, gây ảnh hưởng hệ thần kinh trung ương, hệ tuần hoàn,…
- Làm việc với hóa chất này ở nơi thông thoáng, tránh gây tích tụ khí SO2 – làm khó thở.
- Làm sạch ngay khi hóa chất bị rò rỉ
- Sử dụng với liều lượng cho phép
- Natri Bisulfite có thể phản ứng với nước và tạo ra khí sulfur dioxide. Nếu không kiểm soát tốt, khí này có thể gây ra sự ô nhiễm không khí và có hại cho sức khỏe.
6. Cách Bảo Quản Đối Với NaHSO3 – Sodium Bisulfite
- Natri bisulfite cần được lưu trữ nơi khô ráo, thoáng mát, tránh xa ánh nắng và các nguồn nhiệt trực tiếp từ môi trường bên ngoài.
- Tuyệt đối không được để Sodium bisulfite gần các chất không tương thích như chất oxi hóa, kiềm.
- Sau khi sử dụng NaHSO3 phải đậy nắp kỹ, tránh để hóa chất thoát ra ngoài, hay để không khí lọt vào trong nhằm không gây ảnh hưởng môi trường và đảm bảo chất lượng sản phẩm.
